2018.12.17

ダイエットという蟻地獄――最新の医学データが示すダイエットの真実(2)
蟻地獄――ダイエッティングサイクルと脱抑制
前回は、周囲の賞賛を求めて過激な目標設定に向かってダイエットをするのと、生活全体を健康的にして、健全なライフスタイルを地道に営み、その結果として健康的な体重になるのが、まったく別なことであると説明してきました。
頑張ってダイエットする、つまり意識的に摂取量を大幅に下げると、饑餓状態に陥り空腹感が強くなります。早晩、その強烈な空腹感、飢餓感に抗しきれず食べ過ぎに陥り、ダイエットに失敗したと意気消沈し、ふたたび厳しいダイエットに励みます。Neumark-Sztainer博士(Neumark-Sztainer & Loth, 2017)が指摘したように、この負のサイクル、ダイエッティングサイクルによって、不健康なダイエットが体重増加につながる可能性があります。
さらなる可能性として、生理的なもの(空腹と満腹の内部サイン)ではなく意志によって摂取量をコントロールしようとすると、禁止している食物を少し摂取しただけで食べ過ぎに至るなど、ダイエットによって脱抑制のリスクが増すとされています。これはPolivyとHerman(Polivy & Herman, 1985; Polivy & Herman, 1995)が1985年に提唱して以来、いくつもの研究がされてきました。
ダイエットのために、身体的・生理的な空腹と満腹の内部サインをずっと無視し続けると、正常な摂取制御を失ってしまいます。長期ダイエッターでは、自分が太ると思っている食物を少しでも摂ると、もう抑制が効かなくなり、食べ過ぎてしまいます。痩せすぎを目指し、限り無く低い摂食量を計画するのですが、実情は間欠的摂取量制限になってしまっています。ずっと食べ物のことばかり考えてしまい、食べ物中毒に陥ってしまっています(Polivy & Herman, 1995)。
現代社会は食べ物への誘惑に満ちあふれています。TVドラマには食事シーンがありますし、旅行番組では各地の名物料理が登場します。何よりテレビコマーシャルは、食べ物ばかりです。テレビを見ているだけで、思わず抑制が取れて食べ過ぎてしまいます(Polivy & Herman, 1995)。仕事・学業にも影響が出ます。ダイエットにより集中力が減り、何か気をそらせるものがあると、すぐに仕事・勉強から気持ちがそれてしまいます。感情的で気持ちが安定せず、両極端に振れやすく、不機嫌となりやすく自分を抑制できなくなり、そんな自分のことが嫌いになってしまします。
迫り来る飢餓感、強い空腹感に耐え抜くことは、人間が生物である限り不可能です。健康的なライフスタイルを旨として、地道に平穏な日々送り続けることで、健康的な体重に到達することが可能です (Wing & Phelan, 2005)。
もっとも恐ろしい結末、太り易い体質
もっとも恐ろしいことは、ダイエットとリバウンドを繰り返すことで、たんに体重が戻るだけではなく、太り易い体質も獲得してしまうことです(Blomain, Dirhan, Valentino, Kim & Waldman, 2013; Maclean, Bergouignan, Cornier & Jackman, 2011; MacLean, Higgins, Giles, Sherk & Jackman, 2015)。もう30年も昔から危険性が指摘されており、ヨーヨーダイエットと呼ばれています(Brownell, Greenwood, Stellar & Shrager, 1986)。動物実験でダイエットを繰り返すと、食物を身体に貯める能力が向上し、少しの食物で体重が上がってしまうことが証明されています(Brownell, Greenwood, Stellar & Shrager, 1986)。これは身体の仕組みから考えれば当然です。飢饉を経験するほど、飢餓に強くなるからです。
人間の身体にはホメオスターシスといって、色々な外的危険から身体を護り、身体の状態を一定にしようとするメカニズムが備わっています。身体にとっては寒冷とともに、飢餓状態は生命最大の危機ですから、それに対抗しようとするのは当然で、ダイエットとは、その飢餓状態に意識的に陥れようとしているのですから、身体が抵抗して当然です。
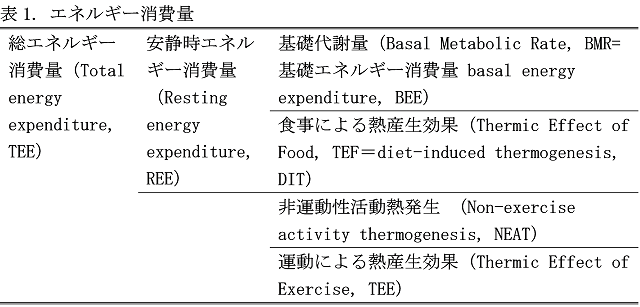
ここで、身体のエネルギーの基礎について少し説明します(表1)。
1日の総エネルギー消費量は(1)基礎代謝量、(2)運動による熱産生効果、(3)非運動性活動熱発生、(4)食事による熱産生効果の4つの合計です。この総エネルギー消費量より多いカロリーを食事により摂取すると、余ったエネルギーを筋肉や脂肪として貯蔵し、体重は増加しますし(アナボリック)、摂取カロリーが少ないと、それらをつぶして使用して、体重は低下します(カタボリック)。そして体重低下の時には、(1)基礎代謝量、(2)運動による熱産生効果、(3)非運動性活動熱発生、(4)食事による熱産生効果の4つとも低下しますが、それを適応熱産生(adaptive thermogenesis)と呼びます。
基礎代謝量は、肺(呼吸)、心臓・血管(循環)、脳・神経(認知)などの生理機能や熱産生(体温の維持)、排泄を営むために必要な最小限のエネルギー量です。普通の日常生活では、総エネルギー消費量の約60%が基礎代謝量です(田中喜代次、中田由夫, 2017)。基礎代謝量は、(1)約12時間以上の絶食、(2)安静仰臥位で筋の緊張を最小限にした状態、(3)快適な室温で心身ともにストレスの少ない覚醒状態で測定されます(田中喜代次、中田由夫, 2017)。したがって、絶食状態で測られた基礎代謝量に、食事による熱産生効果を足した数字が、安静時エネルギー消費量(resting energy expenditure , REE)とされています。
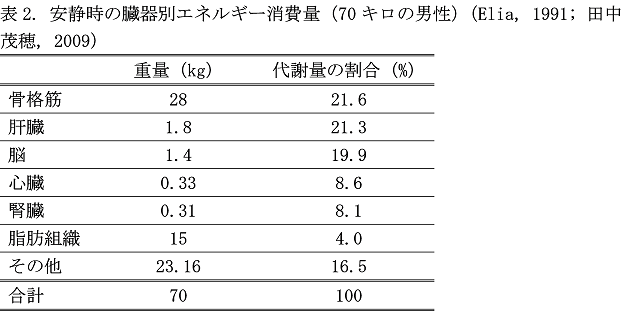
安静時エネルギー消費量のうち、各臓器・組織別のエネルギー消費量をみてみますと骨格筋が2割です(表2)。運動選手では骨格筋が25~40%と、最大部分を占め、運動選手は骨格筋の量が大きく、その結果、基礎代謝も高くなります。一方で、除脂肪量が同じでも(脂肪の量が増えていなくとも)、高齢になるにつれて基礎代謝は低下します。
体重低下とともに代謝も下がってしまいます。そこで、代謝を下げずに、太り易い体質にならずに減量をしたいと考えてしまいます。田中喜代次先生によると、それは非常に困難です(田中喜代次、中田由夫, 2017)。そのためには、筋タンパクの分解よりも合成が上回るように、(1)おおよそ体重1 kgあたり1.5~2 gのタンパク質の摂取、(2)筋肉の限界の80%程度の力を入れて短時間に繰り返して行う高強度レジスタンストレーニングを行うようにしながら、一方、脂肪の蓄積よりも分解が上回るように、(3)長時間の有酸素性運動と(4)糖質制限を行うことです。
ボディビルダー選手たちは、毎日「1日に卵を5~6個も食べ、間食にチーズのかたまりを摂り、牛乳を2~3リットルも飲み」ながら、「毎日、何時間ものトレーニングに励む」ことになります(田中喜代次、中田由夫, 2017)。このようなハードなトレーニングは、オーバートレーニングとなる可能性があります。
事実、「脊椎、関節、腱、筋肉などの損傷」(場合によっては後遺症が残る)、「倦怠感、著しい疲労感、労働意欲の減退、睡眠の質の低下、心臓の拡張、心臓の肥大、不整脈、女性での生理不順や無月経、貧血(sports anemia、スポーツ貧血)、二次性多血症」の可能性があり「健康的な行為とは言い難い」のです(田中喜代次、中田由夫, 2017)。
また、体重を下げながら代謝を上げることは、日常生活を普通に続けながら行うことはできません。仕事・学業を棚上げにして、極端な食生活と非常に過酷なトレーニングだけで毎日が終わることになります。まさに非現実的な目標なのです。
ダイエットによって脂肪細胞数が増える
さらには、ダイエットして体重減少して、リバウンドして体重が元に戻るたびに、脂肪細胞の数が増えてしまう可能性が指摘されています(Maclean, Bergouignan, Cornier & Jackman, 2011; MacLean, Higgins, Giles, Sherk & Jackman, 2015; 黒田雅士, 中川香澄, 阪上浩, 2016)。
脂肪組織は余剰のエネルギーを中性脂肪のかたちで細胞内部に蓄積します。そして、必要に応じて貯蔵している中性脂肪を分解、遊離脂肪酸として細胞外に放出することで、他の臓器にエネルギー供給を行います。そのため、ダイエットなどによって摂取カロリーが、身体が必要とするカロリーを下回り体重減少が始まると、脂肪組織は中性脂肪を放出して、細胞の大きさが小さくなっていきます。しかし、小さくなるだけで、細胞数は減らないため、身体が貯蔵できる最大中性脂肪量は変わらないままなのです。
そして生理的に生ずる(正常な身体の反応として湧いてくる)飢餓感に抗しきれず、ふたたび通常に摂取するようになると、脂肪組織が中性脂肪を貯蔵し、1つ1つの細胞が大きくなるだけではなく、新規脂肪組織が形成・増殖し(脂肪細胞の総数が増える)、結果として、貯蔵できる最大中性脂肪量が増加してしまう可能性が指摘されています(Maclean, Bergouignan, Cornier & Jackman, 2011; MacLean, Higgins, Giles, Sherk & Jackman, 2015)。
体中のホルモンが健康を守っている
身体中のホルモンも飢餓という危機から人間の身体を護るように働いています。飢餓感、満腹感にはグレリン(ghrelin)、ニューロペプチドY(neuropeptide
Y:NPY)、レプチン(leptin)、インスリン(insulin)、グルカゴン様ペプチド-1 (glucagon-like peptide 1, GLP-1)、甲状腺ホルモンなどが関わっています。順番に説明していきます。
図1(中村和弘 & 中村佳子, 2017)にあるように、脳の奥にある、生物、また哺乳類の一員として基本的な制御を担っている視床下部が、自律神経系を制御しています。摂食を制御しているのが視床下部弓状核のNPY/AgRP(neuropeptide Y/ agouti-related peptide)ニューロン(神経)とPOMC (POMC:proopiomelanocortin)ニューロン(神経)であり、グレリン(飢餓感を)とレプチン(満腹感を)は、1次ニューロンであるこれらニューロンを相反的に調節します。
図1の下部には胃から視床下部へ、飢餓感を伝えるグレリン-ニューロペプチドY(neuropeptide Y:NPY)系が描かれています。空腹となると胃からグレリンというホルモンが放出されます。これが図1の上の部分の視床下部弓状核のニューロペプチドY ニューロン群に作用して興奮させると、視床下部室傍核につながる神経の先(軸索)からニューロペプチドYが放出され、このニューロペプチドYの作用によって飢餓信号が生み出されます(中村和弘, 中村佳子, 2017)。
この視床下部からの飢餓信号によって活性化され、飢餓反応を駆動するGABA作動性ニューロン群が延髄の網様体にあります(中村和弘, 中村佳子, 2017)。この網様体のニューロン群は、飢餓時に交感神経系と運動神経系という2つの異なる出力神経系を同時に制御することによって、エネルギー消費(熱産生)を抑制するとともに、交感神経系・運動神経系を通じてエネルギー源の摂取(摂食)を促進する(動いて捕食する)というユニークな中枢神経回路の中心に位置しています。この神経回路は、つねに飢えとの戦いであった長い進化の過程で哺乳類が獲得した、基本的な生存機能メカニズムと考えられています(中村和弘, 中村佳子, 2017)。そして、このニューロペプチドYは、体重減少により多めに分泌されることが報告されているのです(Essah, Levy, Sistrun, Kelly & Nestler, 2010)。
図1. レプチン、グレリンなどによる食欲調節(中村和弘, 中村佳子, 2017より)
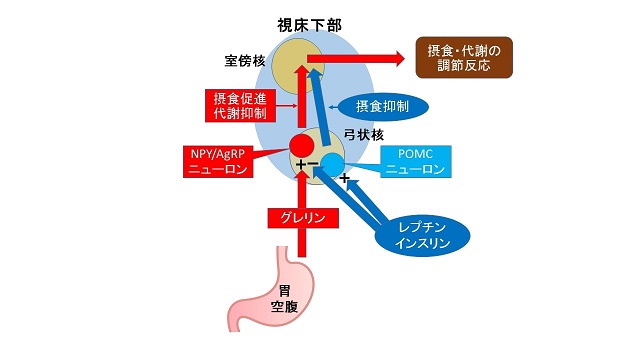
レプチンは1994年に発見された脂肪細胞から分泌される重要なホルモンで、脳の視床下部および報酬系にも働きかけ、食欲をコントロールします。ダイエットを続けるとレプチンは減少し、摂食意欲や渇望感が高まります。具体的にはレプチンが脂肪細胞で特異的に産生、分泌された後、血液を通じて脳に運ばれ、視床下部弓状核のニューロンのレプチン受容体に作用し、弓状核のPOMC/CARTニューロンを活性化して、NPY/AgRPニューロンの活性を抑制します(細田公則 ほか, 2016)。
その結果、摂食が抑制され、エネルギー消費が亢進されます。脂肪量に比例してレプチン分泌量も増加します。脂肪萎縮症という病気では脂肪組織が消失しており、レプチンが産生されませんので、血中レプチン濃度が低下し、食行動異常や糖脂質代謝異常が認められます。レプチン補充療法を行うと、インスリン抵抗性の改善、HbA1c(過去1~2ヶ月の平均血糖値を反映)、血中中性脂肪濃度の低下、脂肪肝の著明な改善をもたらします。
このレプチンも太り易い体質に関連しています。体重減少にしたがってレプチンも低下し、減量した後の体重増加量とレプチンの低下量とに強い相関が認められます(Blomain, Dirhan, Valentino, Kim & Waldman, 2013)。
さらに困ったことに、5%未満の体重減少では、十分にレプチンが低下しなかったことが報告されているのです(Varady, Tussing, Bhutani & Braunschweig, 2009)。抗肥満薬として期待されたこともありましたが、動物実験で食餌性肥満モデル動物や肥満の人では体脂肪量の増加に比例した血中レプチン濃度の上昇を認めるのに肥満のままです。さらにレプチンを投与しても体重減少や代謝改善作用が認められません。そこで、レプチン抵抗性が提唱され、視床下部での変化などが仮定されています(細田公則 ほか, 2016)。
インスリンは三大栄養素である炭水化物、タンパク質、脂質のすべての同化作用(貯蔵を命令する)を有し、炭水化物のなかでもグルコース(俗によく血糖と称されています)に対する反応性が高く、血糖上昇により膵臓からの分泌が促進され、血糖低下によって分泌が抑制されます。また、食事を摂取すると腸からグルカゴン様ペプチド-1 (glucagon-like peptide 1、GLP-1)が分泌され、膵臓に作用してインスリンの分泌を促進し、食後の血糖を低下させます。
さらにGLP-1は、迷走神経を通じて、さらに直接、視床下部に作用し食欲を低下させるらしいのです(Katsurada, et al, 2014)。体重が減少すると、このGLP-1分泌も鈍くなります(Adam, Jocken & Westerterp-Plantenga, 2005)。ただインスリンやGLP-1は「分」~「時」単位で、一方レプチンは「日」単位でエネルギーの過不足を脳に伝えるため、その影響はより継続的です(細田公則 ほか, 2016)。
そのほか、体重減少に伴って代謝をコントロールする甲状腺ホルモンが減少し、コルチゾルが増加し、肝臓でのタンパク質からグルコースへの変換を促進すると同時にタンパク質の分解を亢進させます。
体重減少に伴って飢餓に生き残れるように用意された防衛装置、ホメオスターシスが働き、元の体重に戻ろうとします。人類、300万年の歴史のうち、299万9900年以上は飢餓と背中合わせであったといわれています(石原結實, 2007)。次なる飢餓、飢饉に備えて、より多くのエネルギーを蓄えられるように脂肪細胞数が増加しても、それは、その種族が長く飢饉に耐えて生きてきた証です。
ファーストフードという高脂質、ハイカロリーな食物が安価に手に入る肥満に導かれやすい環境、obesogenic environmentは、この四半世紀に先進各国に出現した生物である人間にとって特殊な環境で、原始人と基本的に同じである生物としての人間にとって、反対の意味で厳しい環境なのです。
地道な生活を営み健康な体重に至る
健康的な生活を地道に営んだ結果、健康な体重を維持できることが分かってきています。本当に身も蓋もない話、しごく当然な話です。1994年にWingとHillは全米体重コントロール成功者登録(National Weight Control Registry)をスタートしました (Wing & Phelan, 2005)。登録できる人は30ポンド(約13.6キロ)の減量を1年以上維持できた18歳以上の男女です。
最初に3つの共通点が見つかりました。(1)控えめな低カロリー・低脂質食を続けていること、(2)運動をきっちりと続けていること、(3)定期的に体重測定を行っていることです。そして最近、さらに4番目のことが分かりました。(4)必ず朝食を摂っていることです。
まず、摂取量は控えめで、毎日の食事は約1800カロリーです。そして、決して羽目を外すことなく、その制限を守り続けていました。女性は週に2545カロリーの、男性は週に3293カロリーの運動を行っていました。これは速歩での歩行運動を毎日、1時間以上していることに相当します。そして毎日のように体重を測定していたのです。
また、4番目の毎日朝食を摂るという習慣が、なぜ有効なのか科学的には解明されていません。ここでいう科学的とはマウスの実験であり、マウスが朝食を摂ったからといって身体の代謝が上昇するわけではないからです。しかし、この分野の権威たちが、ランダム化比較試験で証明されていない、神話でしかない(都市伝説だ)と声明した後(Casazza, et al, 2013)、多くの非難が沸き起こりました(Huber, Halsey & Reeves, 2013)。
一つ、興味深いデータがあります。健康な20歳台の男女を、3食食べる、朝食を抜いて昼夕食を食べる、朝昼の食事を抜いて夕食を食べるという3群に分けて、一日の間のレプチン濃度を測定した研究です。朝食を抜くと、昼ごはんを食べたあとでもレプチン濃度は低く、夕食後の寝る前でもまだ低いままでした。朝昼の食事を抜くと、ずっとレプチン濃度は低く、夕食を食べてもなかなか上昇しません。
レプチン濃度が低いということは、食欲が増加している、つまり脳は栄養を欲しがって食べたがっている状態を示します。この結果は、朝ごはんを抜くと、それだけで、3食食べるよりずっと食欲が高まっている状態が続くことを意味しています。つまり、朝ごはんを抜くとその後で食べすぎてしまう可能性が考えられます。もしかすると、それが朝ごはんを食べている人が太らずにすむ理由かもしれません。過食がある人にまず3食しっかり食べることを勧める理由もここにあります。(Y, Nakamura et al., 2008)。
人間が毎日、まったく同じように行動するためにどうすれば良いのか、ランダム化比較試験やマウスでの実験では解明されません。全米体重コントロール成功者登録のデータは、食品のTVコマーシャルに溢れ、安価に高カロリー、高脂質な食物が手に入るファーストフード店、さらには24時間オープンのコンビニエンスストアが農村部にさえ溢れる現代社会で、どうすれば健康的な体重を維持できるか示唆しています。
雑誌The New England Journal of Medicine (NEJM)は、医学専門誌のなかでもっとも長い歴史を有し、医学会でもっとも権威のある雑誌といって過言ではありません(専門的な話ですが、科学誌はインパクトファクターという、他の論文に引用されたかなどからはじき出される数字によって評価されますが、2017年度のNEJMのインパクトファクターは72.406と、他の有名雑誌Lancetの47.831、JAMAの44.405よりはるかに高いのです)。Kassirer教授は長く編集長(1991~1999年)だったのですが、1998年の編集長としての念頭の所感(一年の計)として、「減量-呪われた病気」を載せています(Kassirer & Angell, 1998)。
多くのアメリカ人が低カロリー・低脂質食、ゼロカロリー飲料を飲み、ダイエット食品を食べ、“fat farm”(直訳すれば太っちょの訓練場、となるでしょう)といった有料フィットネスクラブに入会し、強迫的に運動し、はては脂肪吸引し、抗肥満薬を飲んでいることを嘆いています。300~500億ドル(1998年当時)が「浪費」されています。そして減量に失敗すると、自分を責め罪悪感に苛まれます。
しかし、多くの抗肥満薬がFDAで一旦、認可された後、重篤な副作用が認められ、認可が取り消されています(永田利彦, 2016a; 永田利彦, 2016b)。食欲があることは正常で健康ですから、それを抑える薬は非常に危険なのです。他の病気を有さない肥満で、減量の長寿効果はよく分かっていません。一方で、太っているだけで醜いとさげすまれ、米国では多くの人々が摂食障害に陥り、命を落としています。
そこでKassirer教授は糖尿病、高血圧といった何らかの合併症が無い限り、医師は減量を進めるべきではないとしています。それだけではなく、医師は職場、学校での肥満にたいするさげすみ、いじめに対峙すべきだとしています。それから20年経った今、多くのTVコマーシャル、新聞広告がなされている日本の状況は、その当時の米国を彷彿とさせます。
減量した体重を維持するのは、慎ましやかに地道な生活を営むことが重要です。仕事、学業、趣味の時間を多少、制限・犠牲にしてでも健康を守らなければならないときに、毎日をヘルシーなライフスタイルに変える必要があるのは当然です。見た目重視とはかけ離れた目立たない行為なのです。
次回は、皆さんが目指している体重はじつは痩せすぎ体重であること、若年から摂取制限を行うこと、痩せすぎ体重を維持することが、寿命を縮める可能性が高いことが、最近の研究から判明したことを紹介します。
文献
・Adam, T. C., Jocken, J. & Westerterp-Plantenga, M. S. (2005) Decreased glucagon-like peptide 1 release after weight loss in overweight/obese subjects. Obesity Research, 13, 710-716.
・Blomain, E. S., Dirhan, D. A., Valentino, M. A., Kim, G. W. & Waldman, S. A. (2013) Mechanisms of Weight Regain following Weight Loss. ISRN Obes, 2013, 210524.
・Brownell, K. D., Greenwood, M. R., Stellar, E. & Shrager, E. E. (1986) The effects of repeated cycles of weight loss and regain in rats. Physiology & Behavior, 38, 459-464.
・Casazza, K., Fontaine, K. R., Astrup, A., Birch, L. L., Brown, A. W., Bohan Brown, M. M., et al (2013) Myths, presumptions, and facts about obesity. New England Journal of Medicine, 368, 446-454.
・Elia, M. (1991) The inter-organ flux of substrates in fed and fasted man, as indicated by arterio-venous balance studies. Nutrition Research Reviews, 4, 3-31.
・Essah, P. A., Levy, J. R., Sistrun, S. N., Kelly, S. M. & Nestler, J. E. (2010) Effect of weight loss by a low-fat diet and a low-carbohydrate diet on peptide YY levels. International Journal of Obesity, 34, 1239-1242.
・細田公則, 青谷大介, 日下部徹, 田中智洋, 孫徹 & 中尾一和 (2016)エネルギー摂取の制御機構 ヒトの摂食調節 レプチンを中心に. 実験医学, 34, 279-283.
・Huber, J. W., Halsey, L. G. & Reeves, S. (2013) Myths, presumptions, and facts about obesity. New England Journal of Medicine, 368, 2234-2235.
・石原結實 (2007) 病気を治す食べ方、食べ物. 東京: ベストセラーズ
・Kassirer, J. P. & Angell, M. (1998) Losing weight–an ill-fated New Year’s resolution. New England Journal of Medicine, 338, 52-54.
・Katsurada, K., Maejima, Y., Nakata, M., Kodaira, M., Suyama, S., Iwasaki, Y., et al (2014) Endogenous GLP-1 acts on paraventricular nucleus to suppress feeding: projection from nucleus tractus solitarius and activation of corticotropin-releasing hormone, nesfatin-1 and oxytocin neurons. Biochemical and Biophysical Research Communications, 451, 276-281.
・黒田雅士, 中川香澄 & 阪上浩 (2016)エネルギー代謝の制御機構 脂肪細胞の発生と機能 白色脂肪細胞を中心に. 実験医学, 34, 184-190.
・Maclean, P. S., Bergouignan, A., Cornier, M. A. & Jackman, M. R. (2011) Biology’s response to dieting: the impetus for weight regain. American Journal of Physiology – Regulatory Integrative and Comparative Physiology, 301, R581-600.
・MacLean, P. S., Higgins, J. A., Giles, E. D., Sherk, V. D. & Jackman, M. R. (2015) The role for adipose tissue in weight regain after weight loss. Obesity Reviews, 16 Suppl 1, 45-54.
・中村和弘 & 中村佳子 (2017) 飢餓反応の中枢神経回路メカニズム. 肥満研究, 23, 161-168.
・Y. Nakamura, K.Sanematsu, R.Ohta, S.Shirosaki, et.al(2008)Diurnal variation of human sweet taste recognition thresholds is correlated with plasma leptin levels. 57, 2661–2665 (2008).
・永田利彦 (2016a) 過食性障害の治療. 精神科臨床Legato, 2, 134-138.
・永田利彦 (2016b) 摂食障害の薬物療法-過食性障害を中心に. 精神科, 28, 23-29.
・Neumark-Sztainer, D. & Loth, K. (2017) The impact of dieting. In Eating disorders and obesity : a comprehensive handbook, Third edition (eds K. D. Brownell & B. T. Walsh), pp. 109-115. New York: The Guilford Press.
・Polivy, J. & Herman, C. P. (1985) Dieting and binging. A causal analysis. American Psychologist, 40, 193-201.
・Polivy, J. & Herman, C. P. (1995) Dieting and its relation to eating disorders. In Eating disorders and obesity : a comprehensive handbook (eds K. D. Brownell & C. G. Fairburn), pp. 83-86. New York: Guilford Press.
・田中喜代次 & 中田由夫 (2017) 減量しながら筋肉量および基礎代謝量を高めることは可能か? 体力科学, 66, 209-212.
・田中茂穂 (2009) エネルギー消費量とその測定方法. 静脈経腸栄養, 24, 1013-1019.
・Varady, K. A., Tussing, L., Bhutani, S. & Braunschweig, C. L. (2009) Degree of weight loss required to improve adipokine concentrations and decrease fat cell size in severely obese women. Metabolism: Clinical and Experimental, 58, 1096-1101.
・Wing, R. R. & Phelan, S. (2005) Long-term weight loss maintenance. American Journal of Clinical Nutrition, 82, 222S-225S.
プロフィール

永田利彦
大阪市立大学大学院を修了後、大阪市立大学大学院医学研究科神経精神医学教室講師、准教授、ピッツバーグ大学客員准教授などを経てH25年なんば・ながたメンタルクリニックを開設。医学博士、精神科専門医、精神保健指定医、精神保健判定医、Academy for Eating Disorders、Research Society for Eating Disorder、日本摂食障害学会理事。日本不安症学会、日本うつ病学会、日本生物学的精神医学会、日本精神科診断学会などの学会の評議員。日本摂食障害学会監修・摂食障害治療ガイドライン(2012)の代表編者の1人。摂食障害、不安障害、パーソナリティ障害、気分障害に関する論文、総説多数。

山田恒


