2015.09.30

顕微鏡でも見えない!酵素たちの戦い――セルロースの工業的利用をめざして
木や草などに含まれる「セルロース」。地球上に最も多く存在する有機物であり、古くから有望な生物資源(バイオマス)とされてきた。しかし、バイオ燃料などを生産する際のコストの問題があり、継続的かつ大規模な利用は未だに実現されていない。そんな中、東京大学大学院農学生命科学研究科の伏信進矢教授は、燃料生産の効率化において重要な役割を果たす酵素のしくみを明らかにした。酵素の研究は今後のバイオマス開発にどのような影響をもたらすのだろうか。伏信教授にお話を伺った。(聞き手・構成/大谷佳名)
オイルショックをきっかけに
――なぜセルロースが現在、注目されているのでしょうか。
わたしたちは今、石油や石炭などの化石燃料を燃やしていますよね。あれはおそらく何億年も前の植物や藻のような生き物が積もったのが、長い時間をかけて変成してできたんじゃないかと言われています。
それを、ぼくらは何百年の間にバンバン燃やして使っている。埋蔵量がどれくらいあるかわかりませんが、やっぱりこのままじゃよくないよね、ってみんな思っているわけですよね。それでバイオマス(生物資源)を使おうと考えている人は当然昔からいました。
最初に「ヤバいな」とみんなが気づいたのはオイルショックでした。限界があるのは分かっていたんだけど、値段が上がって初めて危機感を持つわけです。それで70年代には、澱粉やセルロースといったバイオマスの研究が盛んになります。
――なるほど、70年代から注目されていたのですね。
澱粉はトウモロコシなど、セルロースは木や草などの材料なのですが、実はどちらも「グルコース」という糖でできているんです。ただ糖の繋がり方が違うだけで、こんなに性質が違うものになるのです。
また、セルロースを分解する酵素は「セルラーゼ」、澱粉を分解する酵素は「アミラーゼ」と呼ばれます。酵素の名前って、○○を分解するのは「○○アーゼ」って言うんです。
しかし、セルラーゼはアミラーゼと比べて、非常に効率の悪い酵素です。だからコストの面で工業化がなかなか難しい。70年代ごろの段階では実用化はほど遠いと言われていました。結局そうこうするうちに石油の値段が下がって忘れられてしまいました。
――なぜ効率が悪い酵素なのでしょうか。
セルロースをエタノールなどの燃料に加工するには「前処理→糖化→発酵」の過程を踏んでいきます。この「糖化」の段階で、セルラーゼはセルロースに作用し、グルコースの結合を分解します。しかし、木を見たらわかるようにセルロースは固い。このため、分解は簡単ではありません。
セルロースの構造は一本一本の鎖になっているので、まずはこれを剥がさないといけない。一本一本は共有結合という強い結合でできていて、チェーン同士は水素結合でつながっています。
セルロースの水素結合はとても規則正しくたくさん並んでいるので、分子と分子が引き合う力がすごく強くて、ガチガチに固まっているイメージ。なんとかこれを引き剥がせば分解できるんですけどね。
――酵素が弱いというよりも、敵(セルロース)が強いのですね。分解っていうとどのようなイメージなのでしょうか。鋏でチョキチョキ切るような感じですか。
はい、その通りです。でも、セルラーゼにもいくつか種類があります。主な酵素はセロビオヒドロラーゼ(CBH)、エンドグルカナーゼ(EG)などです。(図1)酵素の表面には「活性部位」と呼ばれる溝があり、ここにそれぞれの酵素の特徴が表れています。活性部位の形によって、分解の仕方も違ってくるのです。
CBHの活性部位はトンネル状になっていて、セルロースの表面を流れながら一つ一つ切っていきます。CBHが走るスピードは結構速いんですが、たくさんのCBHを入れても「渋滞」してしまって、動かなくなってしまうことが分かっています。だから時間がかかるんですね。
それに対して、EGは活性部位が溝のようになっていて真ん中からパチンと鎖を切るんですけど、鎖がとにかく剥がれにくいので、なかなかとりつくことができない。

このように、バイオマスの中でもとにかくセルロースは分解しにくかったんです。
可食性バイオマスの問題点
――再びセルロースが注目されるのはどのようなきっかけがあったのでしょうか。
みんなが再び「バイオ燃料がアツい」と思い始めたのは多分2005、2006年くらい。あのころは石油の値段上がりましたよね。そのころにいち早く工業化されたのが、北米にたくさんあったトウモロコシの澱粉を使ったバイオ燃料製造技術でした。当時はまだトウモロコシの値段が安かったのです。
また南米のブラジルでもバイオ燃料の話が盛り上がっていて、当時はアメリカよりも期待されていました。巨大な平野があって、サトウキビがたくさんとれるからです。サトウキビは飲み物などに入っている砂糖に使われたりしますが、その残り(廃糖蜜)に含まれているショ糖などの糖も、燃料の原料として大量に使われました。
澱粉やショ糖などの可食性糖質は、セルロースに比べて圧倒的に分解しやすく、早くから工業化が確立しています。例えば、ヨウ素をいれると澱粉が紫になるのは、ゆるやかならせん状の構造をとっているからです。つまり澱粉はセルロースのように強い結合で固まっていないので、より速く糖になります。
糖化したら、そのあとは発酵です。酵母をグルコースに作用させると、エタノールができますよね。また、他の微生物で発酵させるとブタノールやアセトンなどの別の化合物ができたりします。2006年に僕はアイオワにいたんですけど、一面のトウモロコシ畑の中にでっかい工場があって、プーンとパン酵母の匂いがして……実際に大規模な工業化が始まっていたんです。
しかし問題があって、その後、やはりトウモロコシなどの食料価格が上がりました。バイオエタノール生産の拡大と食料価格上昇にどの程度の因果関係があるのかは分からないのですが、いずれにせよ、どれだけ大量の「食べられる」バイオマスを使っても、僕らが消費しているガソリンや石油由来の燃料の全てはとうてい賄えません。
このような経緯があったので、やはり食料にならないセルロース系のバイオマスを使ったバイオ燃料の開発は重要であることが再認識されました。
例えばトウモロコシでも、芯、茎、葉などの食べられない部分の多くはセルロースなのです。コーンストーバーといって、冬にストーブに入れて燃やしたり、飼料にしたりするんですけど、そんな廃棄している部分を資源として使おうと考えられています。

セルロース分解を効率化する酵素の研究
――先ほどの酵素の説明を聞くと、かちかちな敵を倒すための武器みたいなものが酵素で、酵素それぞれに得意技があるんですね。
そうです。微生物が作っている酵素を使うのですが、セルロースを分解する微生物にも非常に種類が多くあります。カビなんかもそうですし、空気のない場所、沼とかにいるような微生物もいます。それぞれが違った戦略で、別のタイプの酵素を使って分解しています。
あるいは海にいる細菌とかにもそういった酵素を持っているものもありますし。たとえば、海藻類の表面などからも見つかっているサッカロファガス・デグラダンスという菌はセルロースだけでなく様々な糖質を分解する能力を持っています。他にもセルラーゼを持っている菌だと、嫌気性の(空気のないところに住んでいる)バクテリアであるClostridium属(クロストリジウム属)などもあります。
色々なところにセルロースはそれなりにありますし、時間をかけてもゆっくり分解すれば微生物の「餌」になります。微生物の酵素を探せば、また新しいタイプの酵素が見つかるんじゃないか、ということで世界中の人が研究しているのです。
――新しい酵素は度々見つかっているのですか?
水を加えて糖を分解する酵素(糖質加水分解酵素)をグリコシドヒドロラーゼ(GH)と言いますが、この種類はどんどん新しいものが見つかっています。
そもそも、酵素はタンパク質です。タンパク質はアミノ酸が数百個繋がったものですけど、アミノ酸にも20種類あって、その並び方(アミノ酸配列)によってタンパク質の種類と性質が決まります。(例えばDNAに入っている情報はアミノ酸の並びの順番です。)
酵素の種類が非常にたくさんある中で、「この微生物が作るこの酵素とこの微生物が作るこの酵素は似ている」と言えるのは、アミノ酸配列が似ているからです。ですからアミノ酸配列が似ている酵素をそれぞれ分類しましょう、と考えて、フランスの人たちが、GHをファミリーに分類することを始めました。(図2)
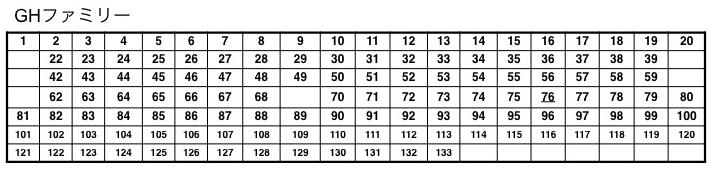
見つけた順に番号がつけられていて、新しいファミリーの酵素はどんどん増えています。僕たちが2004年に出した論文では94番を作りましたが、現在では130を超えています。だから、年に3、4つのペースで見つかっていますね。結構日本人の研究者が新しいファミリーを多く見つけているんです。
――GHファミリー……強そうですね。表の空欄はなんですか?
これは後から別のファミリーに統合されたり、該当しないと判断されたりして削除されたものです。
その一つに、かつて61番というのがあったんですけど、4年ほど前に消されました。これは水ではなく、酸素を使って(入れて)切る酵素だと判明したからです。実はこれは重要な酵素で、通称LPMOと呼ばれ、セルロース系の分解酵素の中では一つのブレイクスルーになりました。
――水で分解するよりも酸素で分解するほうがメリットが大きいんですか?
基本的にセルロースは水の中で分解するので、GHファミリーがメインです。ですが、先ほど言ったように固いのでそう簡単には切れない。酵素をどれだけ使ってもセルロースの表面積は限られていますから、渋滞をし始めて取り付いても取り付いても切れないという状態になります。
そこで、酸素で切れる酵素を入れるんです。LPMOはそんなに切る能力が高い酵素ではないのですが、これをある程度入れるだけで2倍にも3倍にもセルラーゼの活性が上がることが発見されました。これが2010年のことです。これは、先ほど述べたCBHやEGの働きを活性化するブースターである、とノボザイムズ という会社とコペンハーゲン大学の人たちが共同で論文にしたのです。そこから詳しく研究されて、段々その正体が分かってきました。
図3をみてください。これは、微生物の酵素によるセルロースの分解の様子を図にしたものです。
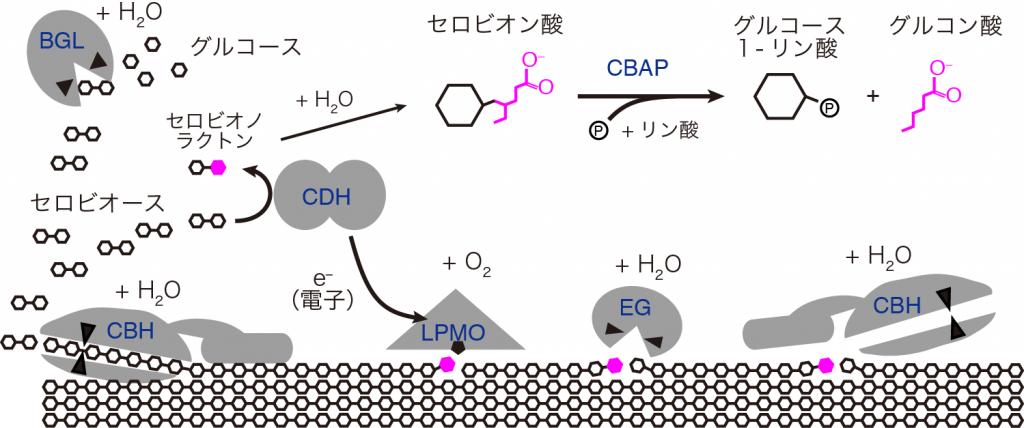
LPMOは平らな表面の真ん中に銅の原子を持っていて、これが酸素と作用して切ります。切ると言っても引っ掻き傷を作る程度なんです。だから活性そのものは強くないし、一秒あたりに切る速度もそんなに速くない。
でも、LPMOはセルロースの平らな表面にもとりつくことができますし、そこに引っ掻き傷をつけることでふわっと表面が緩みます。この緩んだところを取っ掛かりにして、CBHやEGが取り付くことができるようになるわけです。
――真ん中下の三角のやつですね。切り込み隊長のような役割であると。
それと最近明らかになったのが、以前から知られていた酵素でセロビオースヒドロゲナーゼ(CDH)というのがあったんですけど、これがLPMOと共に働いているということ。LPMOは切るときに電子が必要なのですが、どうやら、CDHが電子をわたすことでその分解を助けているのでは、と言われ始めています。
仕組みが明らかにされたCBAPとBGL
――今回、先生方が仕組みを解明した酵素はどのようなものなんですか。
「セロビオン酸ホスホリラーゼ(CBAP)」という酵素です。(図4)これはセルロースが分解されて発酵に移る段階で重要な役割を果たします。
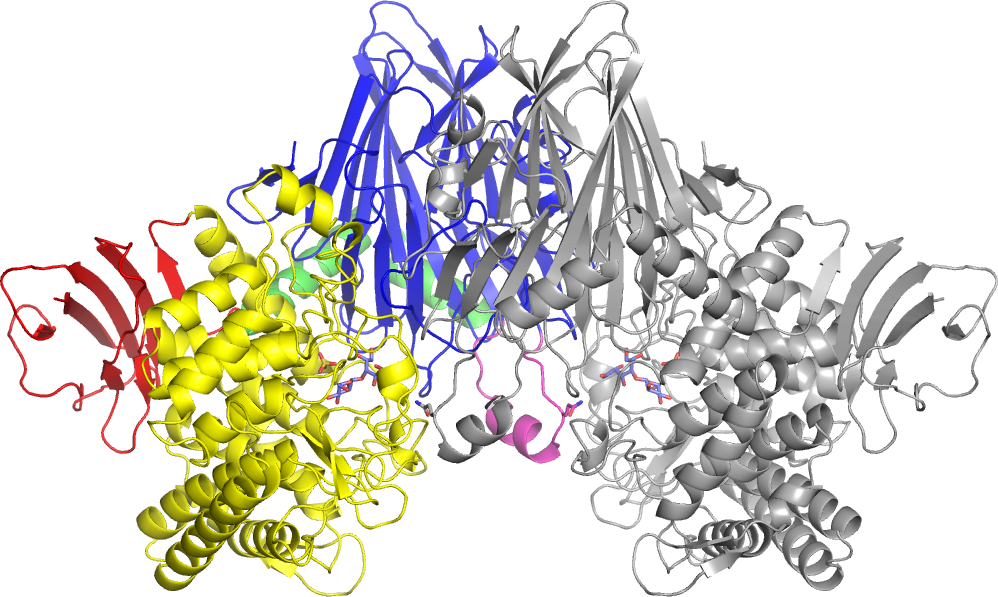
――わっ、すごく複雑な形ですね。
酵素は非常に小さくて、そのまま顕微鏡で覗いても見えないほどです。なので、綺麗に精製して結晶を作り、そこにX線を当てて解析して、その構造を調べます。
――これはどういうものなのでしょうか。
セルロースはCBHやEGによって、グルコースが二つ繋がった「セロビオース」に分解されますが、酵母はこのままでは発酵できません。(図3再掲)

CBHやEGのようなセルラーゼと、それを助ける相棒のような関係であるLPMOやCDHが一緒にはたらくと、セロビオースが酸化されたセロビオン酸という化合物ができます。
このセロビオン酸を分解して、代謝に適した化合物に変化させるのがCBAPです。つまり、エタノールなどの発酵生産へと効率よく導くことができるのです。私たちはCBAPの構造を調べることで、「どのように微生物が発酵につながるプロセスを助けているのか」という重要な情報が得られました。
――ずっと気になっていたんですが、左端の上にある「BGL」っていうのはなんですか。上でちょきちょき何かを切っているようですが。
セロビオースをグルコース二つに分解する酵素で、「β−グルコシダーゼ(BGL)」といいます。(図5)私たちは、2013年にこのBGLの仕組みも明らかにして発表しました。
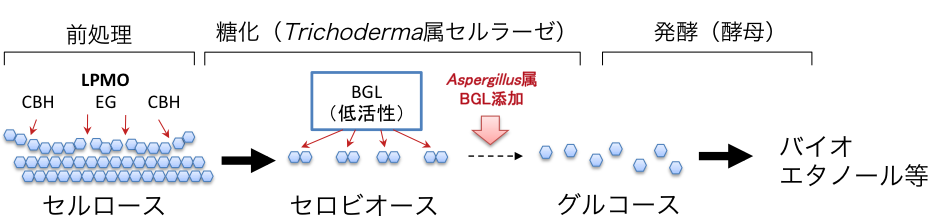
糖化の過程で用いられる、最もコストが低く有望とされているセルラーゼはTrichoderma属(トリコデルマ属)と呼ばれる微生物が作るものです。しかし、これに含まれるBGLがセルビオースを分解する活性は比較的低いことが問題でした。
そこで、セルロースを分解する製剤をつくる際には、Trichoderma属のセルラーゼに、より活性の高いBGLを添加したものが作られています。ここでよく用いられるのはAspergillus属という微生物が作るBGLです。このAspergillus属というのは、お酒や味噌、醤油を作る麹菌(コウジカビ)と同じ仲間なんですよ。(図6)
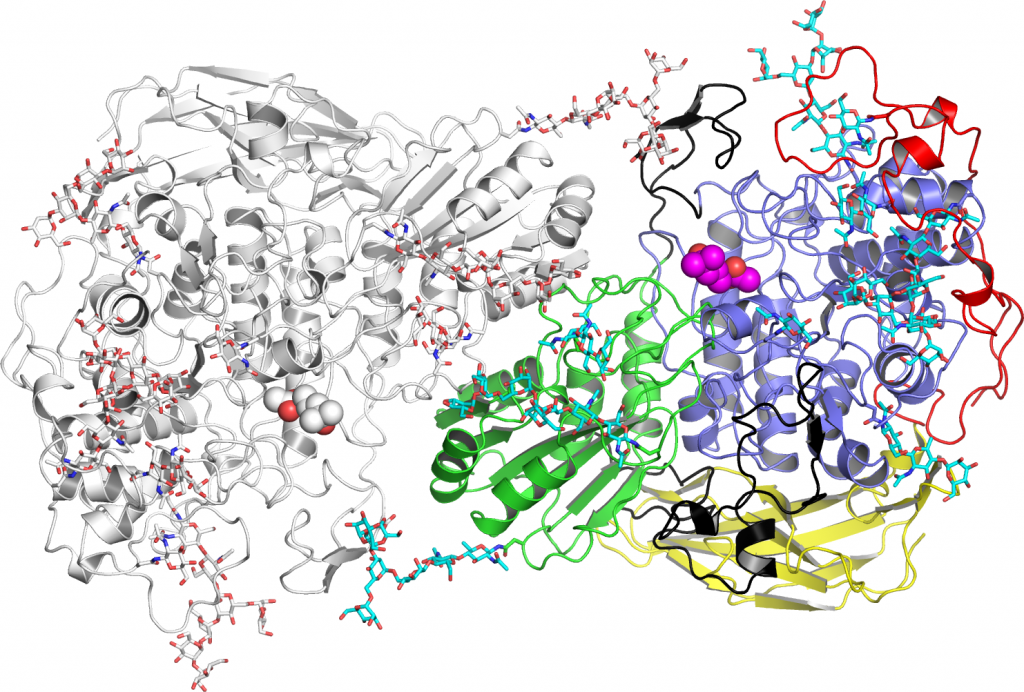
――CBAPの形と全然違いますね。
Aspergillus属のBGLはタンパク質のまわりが糖鎖でおおわれていて、まるで鎧を着ているようでした。この糖鎖の「鎧」がこの酵素を守っているのではないかと考えています。また、この酵素には、セロビオースがぴったりとはまるポケットがあり、セロビオースの分解に適していることも分かりました。
そもそもTrichoderma属は、もともと第二次世界大戦中にアメリカ軍が見つけてきたカビなんです。日本軍を追い詰めていた時に、ブーゲンビル島で木を腐らす菌を発見して、それを持ち帰ったと言われています。その後、これはセルロースをとても効率よく分解するカビだと分かり、今日に至るまでさかんに研究されてきました。
そのため現在では、Trichoderma属は与えられた栄養源のほとんどを使って、全力でセルラーゼを作れるように育種され、工業的に最も多く使われているわけです。
地道な戦いは続く
このように、ここ数年の研究によって酵素によるバイオマスの糖化の能力は大幅に向上しています。また発酵の段階に関しても開発は進んでいます。
たとえば、一般的な酵母はセロビオースやセルロースは発酵できないので、様々な能力を持つ酵母を探してきたり、育種や遺伝子組み換えなどでセロビオースを分解できるようにしようとか、そういう分野はとても進んでいます。
我々が研究しているのは主に糖化と発酵に関わる酵素です。近年では糖化と発酵を同時に行う技術が有効だとされていて、今後はこの二つのプロセスをどのように連携させるかが重要だと考えられています。
――そういった内容も農学部の研究範囲なんですね。
農学部なので応用に近い酵素をやりたいというのもありました。澱粉系の酵素をはじめ、糖関連は工業的に利用されている酵素もたくさんありますし。
今から10年くらい前にバイオマスの研究が最も盛んだったころは、自動車会社やエネルギー系の会社、たくさんの企業が参入してセルラーゼに関する研究をやっていました。現在は当時ほど盛んではないように見受けられますが、それでも、バイオマス分解、特にセルロース系のバイオマス分解は、まだまだ解決すべきイシューがたくさん残されています。
例えば、前処理、糖化、発酵、それぞれの段階で生じるコストをどのように下げていくか。また、セルロース系バイオマスは液体じゃないので、運搬も大変です。森林から木を切ってきて工場に運ぶにしても、それにはある程度広い土地が必要ですし、それを山間部で集積してやるのは、山がちの日本だと相当大変なんですね。
――でも多少は実用化されているのでしょうか。
国内の事情に合わせた、小規模でのバイオマス利用システムの開発は進んでいます。例えば、稲わらのような草本系のバイオマスを利用して、各地域で持続的かつ環境に大きな負荷を与えないようにバイオエタノールを作る方法も模索されています。
また、「バイオリファイナリー」といってバイオ燃料に限らずバイオプラスチックの原料など、他の化成品を生産する技術も期待されています。
プラスチック原料など、エタノール以外の化合物を作るには、酵母をいじればいいのです。「メタボリックエンジニアリング(代謝工学)」といって、酵母の中にある代謝酵素の遺伝子を組み換えれば、目的にあったものを作る酵母を作ることができますし、これはさかんに研究されています。
また、コストを下げるための研究も続いています。しかし、結局石油価格の変動に関わってしまうので、安定的で大規模な実用化にはまだしばらく時間がかかりそうです。
バイオマスの継続的な利用が石油価格に影響されないくらいまで、コスト面で安定的かつ有利なものでないと、社会への貢献にはならないわけですよね。
実際、セルラーゼのブースターであるLPMOのおかげで、酵素の部分に関してはコストが明らかに下がったと言えると思います。また、BGLもコスト低減に関わっていますし、CBAPも酵母に組み込めば、もう少し無駄なく産物が作れるようになるのでは、と期待しています。
そのような地道な作業で、セルロース系バイオマスの分解利用のコストを下げていくことに少しでも貢献できたら、と思っています。
プロフィール

伏信進矢
東京大学大学院農学生命科学研究科教授。1971年広島県呉市生まれ。1994年東京大学農学部農芸化学科卒業。1997年より東京大学大学院農学生命科学研究科助手。1999年博士(農学)取得。2006年米国アイオワ州立大学Visiting Scientist。同大学院助教、准教授を経て2012年より現職。目には見えないほど小さな酵素のはたらき(機能)を、そのかたち(構造)を明らかにすることにより調べている。対象は糖とリン酸に関わる酵素が中心だが、その他のさまざまな酵素についても研究を行っている。農芸化学奨励賞、日本農学進歩賞、日本応用糖質科学会奨励賞、酵素応用シンポジウム研究奨励賞を受賞。


